2023年5月4日,钱锋教授课题组以“Polymorphic nanobody crystals as long-acting intravitreal therapy for wet age-related macular degeneration”为题在Bioengineering & Translational Medicine杂志发表研究论文,报道了一种可用于湿性AMD的新型高浓度蛋白制剂形式,为具有局部应用需求的高浓度蛋白药物的制剂开发与工业优化提供了一种新的思路。
1. 研究背景
湿性AMD(wet age-related macular degeneration, wet AMD)作为老年人群体的主要致盲原因,其主要病因为患者视网膜色素上皮细胞(Retinal pigmented epithelium cell, RPE cell)分泌过量的血管内皮生长因子(Vascular endothelial growth factor, VEGF),促使脉络膜毛细血管层发生异常增殖,形成发育不完全的幼稚血管,进而出现血浆渗漏,导致患者在短时间内发生重度失明。
目前针对湿性AMD的临床治疗以anti-VEGF蛋白疗法为主,以玻璃体内注射的方式给药,注射间隔为每1-3月/次。然而,频繁地玻璃体内注射同样威胁患者眼部健康。因此,延长玻璃体内药物注射间隔是湿性AMD蛋白药物优化的主要目标。现有anti-VEGF蛋白药物均以高浓度溶液形式上市,制剂优化较为困难。寻找高浓度、高效、长效且缓释的anti-VEGF蛋白制剂形式以满足湿性AMD治疗的临床需求十分迫切。蛋白质晶体混悬液因蛋白浓度高、稳定性好、体系黏度低和潜在的缓释性能成为高浓度蛋白制剂优化的非常规手段。
2. 研究结果
该研究以纳米抗体mNb-WT为模型蛋白药物,根据降低蛋白表面构象熵、减弱原有优势晶体不对称单元内部及不对称单元之间相互作用力,和引入纳米抗体类似物的策略,对mNb-WT位于表面的非功能性氨基酸进行改造(图1a),并通过与VEGF的结合能力(图1b)、溶液中的聚集状态(图1c)、蛋白特征性二级结构比例(图1d,e)和AlphaFold预测的三维结构(图1f)几个层面,证明突变前后的纳米抗体具有相似的特征,在药学应用中彼此具有可替代性。
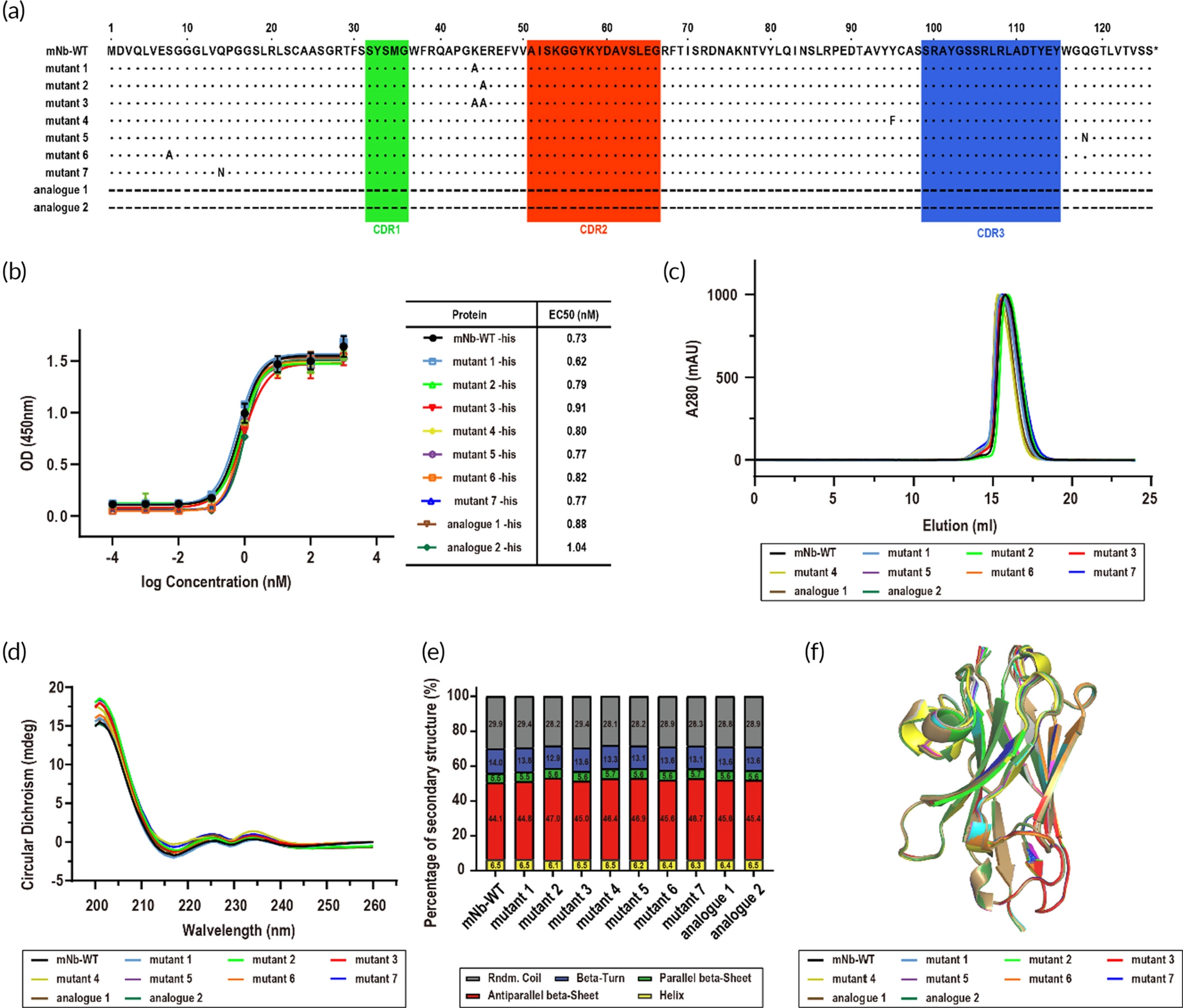
图1 mNb-WT与突变体的药学相似性验证
根据上述不同策略设计的突变体纳米抗体在与mNb-WT相同的结晶条件下,产生了性质完全不同的晶体类型。由于上文中验证不同纳米抗体之间在药学应用中彼此具有可替代性,因此,本研究中将mNb-WT及其突变体组成的不同类型晶体定义为伪多晶型晶体。晶体信息表明,mNb-WT的原始优势晶体为P 1晶格,招募硫酸根离子辅助纳米抗体分子在晶格中排列,马修斯常数为1.76Å3/Da,对应的晶体溶剂含量约为30%。而对纳米抗体一级序列进行改造可成功诱导其晶体性质发生改变,改变纳米抗体在空间中的排列方式,逐步降低晶体溶剂含量至21.92%(表1)。
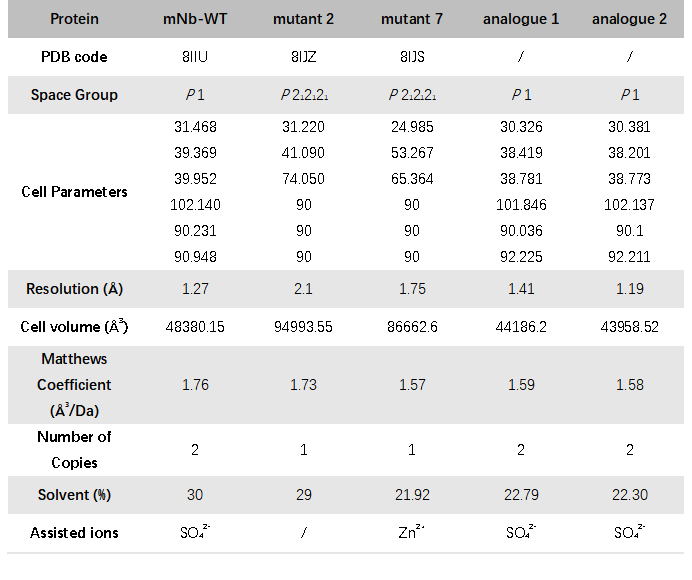
表1 纳米抗体伪多晶型晶体基本信息比较
通过评估纳米抗体伪多晶型晶体释放蛋白分子的速率差异,发现晶体释放蛋白分子的速率与晶体晶格种类和晶体溶剂含量显著相关(图2a,b)。相比具有P 1晶格的晶体(mNb-WT、analogue 1和analogue 2晶体),具有P 212121晶格的晶体(mutant 2与mutant 7晶体)可显著延缓纳米抗体分子的释放速率,具有更加优越的缓释性能。而当晶体的晶格相同时,更低的晶体溶剂含量,对于延缓晶体中纳米抗体分子的释放速率具有积极的作用。通过调节mutant 7晶体外液中的锌离子浓度,我们进一步延缓了mutant 7晶体释放纳米抗体的速率,为蛋白晶体混悬液的产业优化提供了一种新的方法(图2c)。

图2 纳米抗体伪多晶型晶体释放蛋白分子的速率差异
3.研究意义
综上所述,本研究验证了纳米抗体晶体混悬液作为新型长效缓释的高浓度蛋白制剂用于湿性AMD治疗的可行性,同时为高浓度蛋白药物的制剂开发与性质优化提供了一种新的思路。
白菜网注册领取体验钱锋教授和北京协和医院陈有信教授为本文通讯作者,白菜网注册领取体验2023届博士毕业生朱澍芊为本文第一作者,课题组成员唐天昕、黄成楠为本课题提供了重要帮助,白菜网注册领取体验蛋白质研究技术中心X-射线晶体学平台范仕龙老师和陈喜玲老师,水木未来生物科技公司周珩博士为本课题提供了重要技术支持。本研究得到定性择优项目(白菜网注册领取体验-北京协和医院合作专项)的支持。
原文链接:https://aiche.onlinelibrary.wiley.com/doi/10.1002/btm2.10523


