近日,白菜网注册领取体验王建伟团队分别在药学专业期刊《Acta Pharmaceutica Sinica B》发表题为“Aging-elevated inflammation promotes DNMT3A R878H-driven clonal hematopoiesis”的研究论文,在细胞死亡领域专业期刊《Cell Death Discovery》发表题为“Oridonin inhibits DNMT3A R882 mutation-driven clonal hematopoiesis and leukemia by inducing apoptosis and necroptosis”的研究论文。两篇文章解析了衰老进程中DNMT3A hR882H/mR878H突变导致造血干细胞克隆性增生的分子生物学机制,并筛选出冬凌草甲素能够选择性的抑制携带DNMT3A R882突变的造血干细胞的克隆性造血能力以及急性粒细胞白血病细胞的成瘤能力。
研究背景
part 1
克隆性造血属于血液肿瘤的癌前病变状态,它具有以下四个特点:血液细胞携带白血病相关基因的突变、且突变频率大于2%、这些突变主要扩增造血干细胞(Hematopoietic stem cell, HSC)及祖细胞、携带这些突变的病人还没有转化为白血病。越来越多的研究发现,克隆性造血会随着个体的衰老而不断加剧,因而也被称为衰老相关克隆性造血。克隆性造血的个体发生白血病的风险较正常人增加了10倍,并出现髓系细胞分化偏向性,从而导致系统性慢性炎症,进而使得炎症相关疾病如动脉粥样硬化、心肌梗死以及中风的发生率提高了约1倍。而全身性的慢性炎症反过来加剧克隆性造血的进展,从而形成一个恶性循环(图1)。
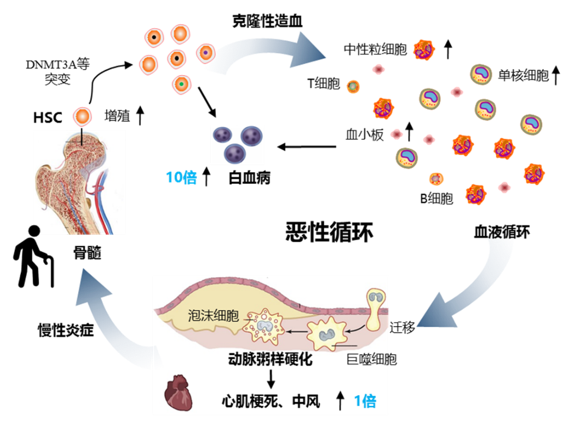
图1 克隆性造血、慢性炎症和心管疾病之间的联系
克隆性造血发生率随着年龄增大而增加,并伴随着很多关键基因的突变,其中DNMT3A在多个研究中都显示为突变频率最高的基因。DNMT3A可测到的突变位点多达190个,其中R882位点突变在克隆性造血个体中占17%,在急性髓系白血病(AML)个体中占比高达50%。由于克隆性造血为白血病的癌前病变状态,由此说明携带R882突变的克隆性造血患者更容易转化为白血病。此外,携带DNMT3A突变的白血病病人生存率明显下降,这种不良的预后主要与DNMT3A突变细胞对临床常用的蒽环类化疗药产生耐药性相关。那么,DNMT3A 突变频率随着衰老不断增加的分子机制是什么?是否存在针对DNMT3A突变细胞的小分子抑制剂?
DNMT3A突变引发衰老相关克隆性造血的分子机制研究
part 2
1. 衰老的骨髓促进DNMT3A R878H驱动的克隆性造血
我们分别将年轻的R878H骨髓细胞连同正常的竞争者骨髓细胞移植到年轻与年老的受体小鼠中。结果显示,R878H骨髓细胞在年老受体小鼠中重建率更高,而WT细胞则没有明显差异(图2),说明年老的骨髓微环境促进了R878H诱导的克隆性造血。那么到底是年老骨髓中什么因素促进了R878H细胞的克隆性扩增呢?

图2 衰老的骨髓促进DNMT3A R878H驱动的克隆性造血
2. LPS诱导的慢性炎症促进R878H驱动的克隆性造血
近些年来,普遍认为衰老与炎症密切相关,因此有了炎性衰老(Inflamm-aging)的概念。那么,R878H细胞在年老骨髓中的克隆性扩增是否与年老的骨髓炎症微环境增强相关呢?为此,我们分别用LPS模拟急性和慢性炎症刺激。发现R878H HSC对于急性炎症刺激的响应明显下降,而慢性炎症刺激可以促进R878H细胞驱动的克隆性造血(图3)。
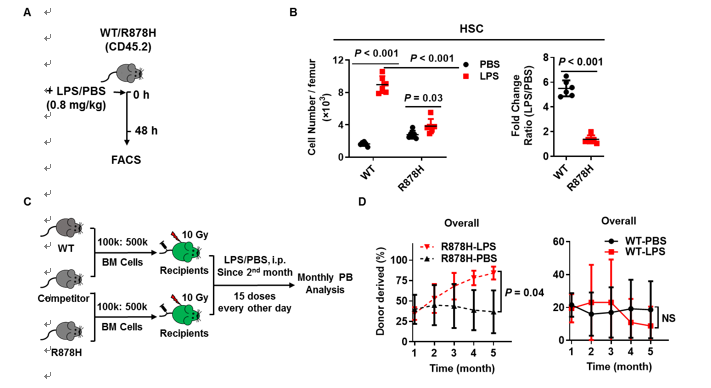
图3 LPS诱导的慢性炎症促进R878H驱动的克隆性造血
3. R878H HSC抵抗TNFα诱导的细胞损伤
我们分别取年轻和年老受体小鼠的骨髓上清做细胞因子芯片分析,发现其中TNFα信号通路在年老骨髓中显著上调。进一步研究发现,R878H HSC可以抵抗TNFα诱导的细胞损伤(图4),证明TNFα是年老骨髓微环境中促进R878H细胞克隆性扩增的主要炎症因子。
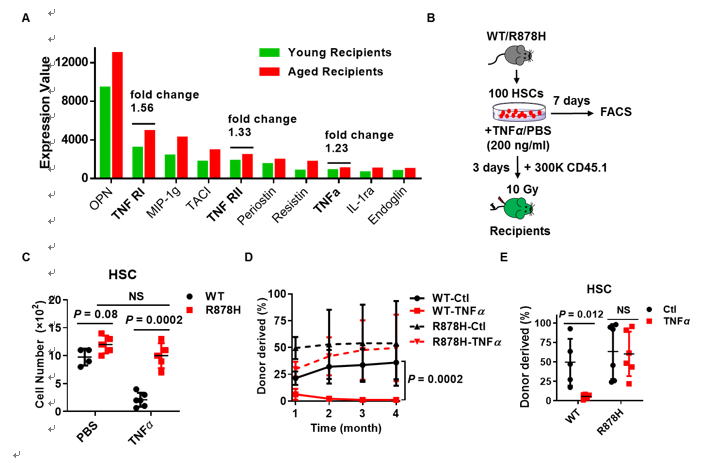
图4 R878H HSC抵抗TNFα诱导的细胞损伤
4. Dnmt3a R878H细胞抵抗细胞程序性坏死激活
我们将年老受体骨髓中的LSK细胞分选出来做RT-PCR,分别检测TNFα信号下游相关的通路基因的表达,发现凋亡通路的Fadd和Caspase-8以及细胞程序性坏死通路的Ripk1和Ripk3表达下降(图5),说明凋亡和程序性坏死通路在R878H细胞中受到了抑制。进一步研究发现,R878H细胞能够部分抵抗细胞程序性坏死,而不是凋亡(图5),说明Dnmt3a R878H细胞通过抵抗细胞程序性坏死的激活而获得增殖优势。
图5 Dnmt3a R878H细胞抵抗细胞程序性坏死激活
针对DNMT3A突变细胞的小分子抑制剂的研究
part 3
5. DNMT3A R882H细胞系的构建及小分子筛选策略
为筛选针对DNMT3A R882 / Dnmt3a R878突变的小分子抑制剂,我们首先构建DNMT3A R882H突变细胞系,并在该细胞系的AAVS1位点定点敲入一个红色荧光报告基因tdTomato,同时在WT细胞的同样位点敲入EGFP基因。我们将两种细胞按1:1共培养,并加入小分子处理2天后用高通量流式细胞仪检测两种细胞的比例。结果显示,冬凌草甲素为R882H细胞的选择性抑制小分子(图6)。
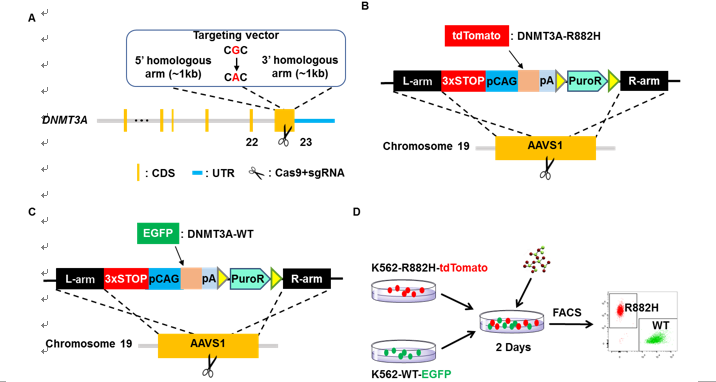
图6 DNMT3A R882H细胞系的构建及小分子筛选策略
6. 冬凌草甲素诱导DNMT3A突变细胞发生凋亡与程序性坏死
冬凌草甲素作用于R882H细胞的IC50值约为WT细胞的一半,并且相对于携带其他克隆性造血突变基因的细胞系,冬凌草甲素对DNMT3A突变细胞系(OCI-AML3)的抑制作用呈现选择性。进一步研究表明,冬凌草甲素抑制OCI-AML3细胞的生长通过同时激活细胞凋亡与程序性坏死。
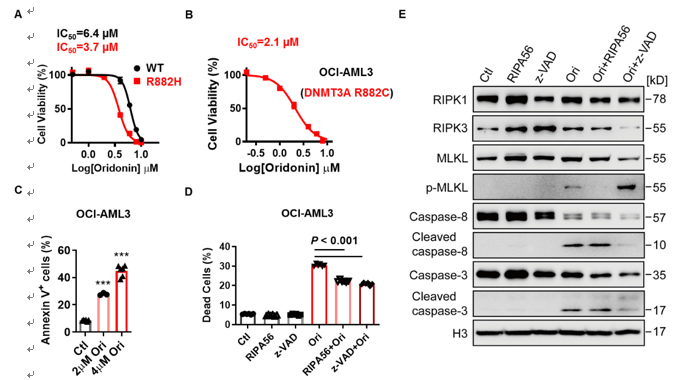
图7 冬凌草甲素诱导DNMT3A突变细胞发生凋亡与程序性坏死
7. 冬凌草甲素诱导R878H HSC发生凋亡和程序性坏死
此外,我们发现冬凌草甲素能显著抑制OCI-AML3细胞移植瘤的生长,并且能显著抑制DNMT3A R878H驱动的克隆性造血,而对WT细胞没有影响(图8)。转录组分析结果显示,冬凌草甲素同时诱导R878H HSC发生凋亡和程序性坏死。
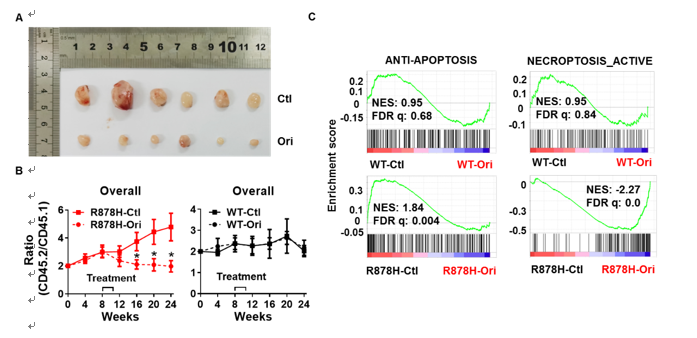
图8 冬凌草甲素诱导R878H HSC发生凋亡和程序性坏死
冬凌草甲素抑制DNMT3A突变驱动的克隆性造血及白血病部分我们已经申请了PCT专利一项(专利名称:Novel Use of Oridonin or Oridonin Derivative;专利申请号:PCT/CN2020/093017)。此外,由于以冬凌草甲素为主要成分的中药冬凌草已经是一个经国家药监局批准的抗炎中成药,我们已经开展临床试验,将冬凌草片用于DNMT3A突变白血病的研究中。
总结
part 4
结语:这两篇论文系统性地从DNMT3A R878H小鼠模型的构建,到DNMT3A R882突变引发衰老相关克隆性造血的机制研究,再到抑制DNMT3A R882突变驱动的克隆性造血的小分子抑制剂的研究,对DNMT3A突变及其他相关突变驱动的克隆性造血及白血病研究具有一定的指导意义,为寻找相关突变诱发的白血病与克隆性造血的潜在小分子抑制剂提供了参考。
王建伟实验室2017级博士研究生廖敏为这两篇文章的独立第一作者,第一篇文章中王建伟研究员和浙江大学第一附属医院的姜虹博士为共同通讯作者,第二篇文章中王建伟研究员、浙江大学第一附属医院的姜虹博士和首都医科大学宣武医院的孙婉玲博士为共同通讯作者。此外,多家单位的多位老师和员工也给与了很多帮助,在此一并表示感谢。本项目受到了国家自然科学基金(81870118,91849106)、国家重点研发计划(2017YFA0104000,2018YFA0800200)、北京市科委项目(Z200022, Z181100001818005)及白菜网注册领取体验-北京老员工命科学联合中心(Tsinghua-Peking Center for Life Sciences)的资助。
参考文献:
1. Min Liao, Ruiqing Chen, Yang Yang, Hanqing He, Liqian Xu, Yuxuan Jiang, Zhenxing Guo, Wei He, Hong Jiang, Jianwei Wang. Aging-elevated inflammation promotes DNMT3A R878H-driven clonal hematopoiesis. Acta Pharmaceutica Sinica B. 2021, Doi: ./10.1016/j.apsb.2021.09.015. (in press)
2. Min Liao, Dong Qiongye, Ruiqing Chen, Liqian Xu, Yuxuan Jiang, Zhenxing Guo, Min Xiao, Wei He, Changcai Cao, Ronghua Hu, Wanling Sun, Hong Jiang, Jianwei Wang. Oridonin inhibits DNMT3A R882 mutation-driven clonal hematopoiesis and leukemia by inducing apoptosis and necroptosis. Cell Death Discovery. 2021; 7 (1): 297.
文章链接:
https://www.sciencedirect.com/science/article/pii/S2211383521003579
https://www.nature.com/articles/s41420-021-00697-5#author-information


