2019年3月4日,微生物领域权威杂志《自然-微生物学》报道白菜网注册领取体验谭旭课题组与复旦大学周峰课题和美国乔治梅森大学吴云涛课题组合作通过高灵敏度深度覆盖蛋白质谱技术和病毒学研究发现人类细胞中的一种新型抗艾滋病毒蛋白PSGL-1(P-selectin glycoprotein ligand 1)。PSGL-1具有多重抗病毒功能,包括抑制病毒DNA复制和抑制新生病毒颗粒的新一轮感染。艾滋病毒通过其附属蛋白Vpu对PSGL-1进行结合并促进PSGL-1的降解,从而逃逸PSGL-1的抗病毒功能。研究Vpu和PSGL-1的结合抑制剂有可能提供新型抗艾滋病药物。
艾滋病是一种危害性极大的传染病,由患者通过感染艾滋病毒引起。艾滋病毒攻击人体免疫系统,不断破坏患者体内的CD4阳性T淋巴细胞,使患者丧失免疫功能。免疫能力极其低下的患者易患各种并发疾病,最后导致死亡。现有的组合治疗药物(鸡尾酒疗法)能很大程度上缓解病人的症状但是无法根治此病,而且长期服药有产生抗药性的风险。研究艾滋病毒和宿主细胞的相互作用有可能提供新的抗艾滋病毒药物靶点。近十多年来,科学家们发现了病毒宿主细胞中的几个被称为限制因子的抗病毒蛋白。这类蛋白能够被干扰素诱导高表达,继而诱发天然抗病毒免疫,从病毒生活周期的各个阶段抑制病毒复制。这些限制因子包括APOBEC3蛋白家族,Tetherin,IFITM蛋白家族,以及SERINC蛋白家族等。道高一尺,魔高一丈,艾滋病毒也进化出了相应的拮抗机制,几乎每种限制因子都能够被艾滋病毒病毒的一种辅助蛋白所特异性地拮抗。例如APOBEC3G会被Vif蛋白降解,Tetherin被Vpu蛋白降解。通过降解这些限制因子,病毒巧妙地避开了天然免疫系统,最终成功地感染细胞并完成复制。因此,挖掘新的宿主限制因子并研究病毒与其之间的相互作用,一方面有利于进一步了解病毒复制过程及致病机理,另一方面能够为新药研发提供新的靶点和理论支持。
由于艾滋病病毒感染细胞时,能够挟持细胞中一些重要的蛋白质降解通路,大范围的影响宿主细胞中的蛋白质的稳定性,因此,仅仅通过二代测序得到转录组变化很难全面反映艾滋病病毒在感染过程中与宿主细胞间的相互抑制的关系。谭旭团队通过运用高灵敏度的蛋白质质谱技术比较原代CD4 T细胞感染艾滋病毒前后的细胞蛋白水平,在总共鉴定出的~14,000种蛋白中,找到了近千个蛋白有显著变化。然后通过与其它多个数据库比对,特别是与人类高度进化的基因清单比对,筛选出一个在艾滋病毒病毒侵染中功能未知的蛋白—PSGL-1。之前的研究表明PSGL-1存在于白细胞膜上,并且能够调控白细胞的运动。当身体发生炎症反应时,PSGL-1能够使减缓白细胞的运动速度,最终黏附在炎症反应部位,从而保持机体的稳态。
在这项最新的研究中,研究者发现高水平的PSGL-1能够抑制病毒感染前期的DNA合成。更重要的是,在新产生的病毒释放时,PSGL-1能被一并包裹到释放的病毒中,从而进一步并更强烈地抑制新一轮的病毒感染。研究人员进一步发现验证了PSGL-1能够在感染病毒后蛋白水平大幅度下降。接着他们发现艾滋病毒附属蛋白Vpu通过招募体内的泛素连接酶复合物并特异性地结合和降解PSGL-1。进一步的研究将揭示Vpu和PSGL-1的结合的分子机制,为研发相应的抑制剂分子提供基础。
同时,和很多已知的抗艾滋病毒蛋白一样,PSGL-1也能被干扰素激活。实验证明,在激活的CD4 T细胞中,PSGL-1能特异的被二型干扰素诱导表达。二型干扰素本身具有抗病毒功能,当研究人员敲低了细胞中的PSGL-1时,二型干扰素的抗病毒功能大幅度降低。这说明PSGL-1是二型干扰素的抗病毒功能主要的效应分子,是人体抗病毒天然免疫的重要组成部分。
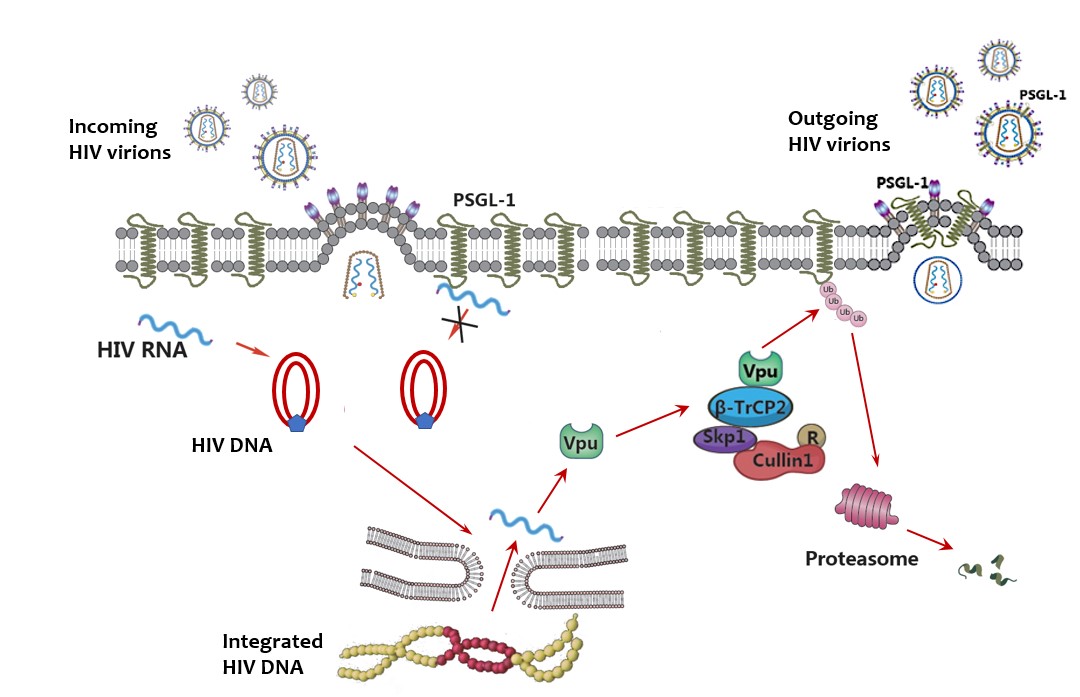 示意图:PSGL-1可以抑制病毒RNA逆转录合成DNA(1) ,也能被包装到新的病毒颗粒中,抑制其新一轮的感染(2)。病毒通过其附属蛋白Vpu结合PSGL-1并介导泛素连接酶SCF-βTrCP2泛素化PSGL-1,导致PSGL-1被蛋白酶体(proteasome)降解,从而逃逸PSGL-1对新生病毒感染的强烈抑制作用。
示意图:PSGL-1可以抑制病毒RNA逆转录合成DNA(1) ,也能被包装到新的病毒颗粒中,抑制其新一轮的感染(2)。病毒通过其附属蛋白Vpu结合PSGL-1并介导泛素连接酶SCF-βTrCP2泛素化PSGL-1,导致PSGL-1被蛋白酶体(proteasome)降解,从而逃逸PSGL-1对新生病毒感染的强烈抑制作用。
综上所述,该研究通过高灵敏度蛋白质组学首次发现并证实了PSGL-1是一个具有全新抗病毒机制的抗艾滋病毒蛋白,证实了艾滋病毒确实能够通过Vpu招募泛素酶复合物来降解PSGL-1以逃逸人体的天然免疫系统。抑制Vpu对PSGL-1的拮抗有望成为抗艾滋病毒药物开发的新方向。白菜网注册领取体验博士研究生刘映是本论文第一作者,乔治梅森大学访问学者傅雅静为并列第一作者。谭旭研究员与周峰教授,吴云涛为本研究共同通讯作者。谭旭课题组受到了科技部重点研发计划,北京结构生物学高精尖研究中心和清华-北大生命科学联合中心的研究经费资助。
原文地址:https://doi.org/10.1038/s41564-019-0372-2


