王建伟博士以造血干细胞衰老为主要研究领域,应用CRISPR/CAS9筛选和早衰动物模型等技术手段来探寻造血干细胞衰老的分子生物学机制以及延缓其衰老的方法。具体研究方向包括:1)揭示造血干细胞自我更新的分子生物学机制;2)揭示造血干细胞衰老的分子机理;3)阐明衰老的造血干细胞向淋系细胞分化能力下降的分子机制; 4)研究衰老的造血干细胞克隆性增生的分子生物学机制;5)利用小分子筛选技术来寻找能够延缓造血干细胞衰老的小分子。
王建伟研究员应用端粒酶衰老动物模型以及shRNA体内筛选技术发现了导致造血干细胞衰老的分子机制:DNA损伤诱导的分化节点Batf导致造血干细胞在衰老过程中重建造血系统的能力下降以及分化为淋系细胞的能力下降;王建伟研究员还发现端粒酶的缺失所导致的累积在造血干细胞内的大量DNA损伤限制造血干细胞进入细胞周期,从而使其长期处于静息状态,即使受到IFNa的刺激,只有累积少量DNA损伤的造血干细胞能够进入细胞周期,并且在进入周期后被修复或进入程序性死亡;通过筛选肿瘤抑制基因,王建伟研究员发现基因Per2在衰老过程中上表达,抑制Per2能够提高造血干细胞的功能,并且能够提高衰老的造血干细胞向B细胞分化的能力,衰老的Per2缺失小鼠的机体免疫能力显著高于野生型小鼠,而且延长了小鼠的寿命。王建伟研究员的这些研究成果对于探寻造血干细胞衰老的分子机制提供了新的方向。
研究成果
建立了在造血肝细胞水平上进行体内筛选的系统
图一:体内shRNA筛选流程
发现造血干细胞分化是其衰老的新机制

图二:作为Cell封面文章发表的王建伟研究员的研究结果表明分化节点在造血干细胞衰老中的作用
发现了生物周期基因Per2的缺失能够提高造血干细胞重建系统的能力并能延缓衰老
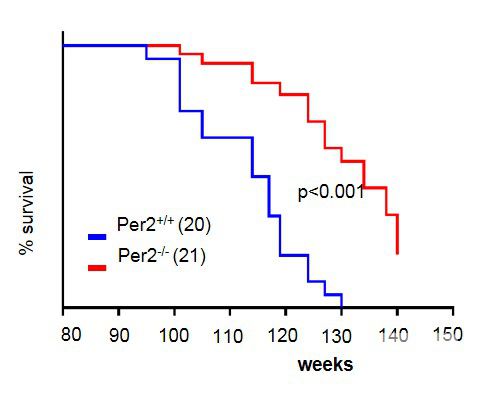
图三:生物周期基因的缺失延长小鼠寿命
代表性论文
1. Hanqing He, Panglian Xu , Xiaofei Zhang , Min Liao , Qiongye Dong , Tingting Cong , Baixue Tang , Xiuxiu Yang , Maoqing Ye , Ying-Jun Chang , Weihua Liu, Xiaowo Wang, Zhenyu Ju,
Jianwei Wang#. Aging-induced IL27Ra Signaling Impairs Hematopoietic Stem Cells. BLOOD. 2020;136(2):183-198.
2. Xiuxiu Yang, Liang Ge,
Jianwei Wang#. BECN1 modulates hematopoietic stem cells by targeting Caspase-3-GSDME-mediated pyroptosis. BLOOD Science. 2020, in press.
3. Hanqing He, Yuqian Wang,
Jianwei Wang#. ALKBH3 is dispensable in maintaining hematopoietic stem cells but forced ALKBH3 rectified the differentiation skewing of aged hematopoietic stem cells. BLOOD Science. 2020;2(3):89-99.
4. Min Liao,
Jianwei Wang#. Tcf12 balances the reconstitution and differentiation capacity of hematopoietic stem cell. BLOOD Science. 2020, in press.
5. Xiuxiu Yang, Tingting Cong, Hanqing He,
Jianwei Wang#. GSDME maintains Hematopoietic Stem Cells by Balancing Pyroptosis and Apoptosis. BLOOD Science. 2020, in press.
6. Min Liao &
Jianwei Wang#. Mechanisms of hematopoietic stem cell ageing and targets for hematopoietic tumour prevention. Adv. Exp. Med. Biol. 2018;1086:117-140.
7.
Jianwei Wang, Yohei Morita, Bing Han and Karl Lenhard Rudolph. Per2 induction limits lymphoid-biased hematopoietic stem cells and immune function in the context of DNA damage and aging. (
Nat Cell Biol. 2016 May;18(5):480-90)
8.
Jianwei Wang, Xin Lu, Vadim Sakk, Christoph A. Klein, and Karl Lenhard Rudolph. Senescence and apoptosis block hematopoietic activation of quiescent hematopoietic stem cells with short telomeres.
Blood. 2014 Nov 20;124(22):3237-40.
9. Tobias Sperka*,
Jianwei Wang* & K. Lenhard Rudolph. DNA damage checkpoints in stem cells, aging and cancer.
Nature Reviews Molecular Cell Biology. 2012; 23:579-590. (*Equal contribution)
10.
Jianwei Wang, Qian Sun, Yohei Morita, Hong Jiang,,, K. Lenhard Rudolph. A differentiation checkpoint limiting hematopoietic stem cell self-renewal in response to DNA damage.
Cell. 2012;148(5):1001-1014.
11.
Jianwei Wang, Hartmut Geiger, K. Lenhard Rudolph. Immunoaging induced by hematopoietic stem cell aging.
Current Opinion in Immunology. 2011;23(4):532-536.
12.
Jianwei Wang*, Hu Wang*, Jingzhou Chen, Xiaojian Wang, Kai Sun, Yibo Wang, Jizheng, Hui Rutai. GADD45B Inhibits MKK7-induced Cardiac Hypertrophy and is Associated with Hypertropic Cardiomyopathy.
Biochem Biophys Res Commun. 2008; 372(4):623-628. (*Equal contribution)
13.
Jianwei Wang, Fu Chunyan, Hui Rutai. The Potential Role of GADD45-βGene in the Development of Hypertrophic Cardiomyopathy.
Molecular Cardiology of China. 2005;5(4):616-618.
14. Zhangfa Song,
Jianwei Wang, Luis Miguel Guachalla, Grzegorz Terszowski, Hans-Reimer Rodewald, Zhenyu Ju, and K. Lenhard Rudolph. Alterations of the systemic environment are the primary cause of impaired B and T lymphopoiesis in telomere-dysfunctional mice. BLOOD. 2010;115(8):1481148-9.
15. Hong Jiang, Eric Schiffer, Zhangfa Song,
Jianwei Wang, Petra Zürbig, Kathrin Thedieck, Suzette Moes, Heike Bantel, Nadja Saal, Justyna Jantos, Meiken Brecht, Paul Jenö, Michael N. Hall, Klaus Hager, Michael P. Manns, Hartmut Hecker, Arnold Ganser, Konstanze Döhner, Andrzej Bartke, Christoph Meissner, Harald Mischak, Zhenyu Ju, and K. Lenhard Rudolph. Proteins induced by telomere dysfunction and DNA damage represent biomarkers of human aging and disease.
Proc Natl Acad Sci U S A. 2008;105(32):11299–04.
16. Shuxia Wang, Yubao Zou, Chunyan Fu, Xiqi Xu, Jizheng Wang, Lei Song, Hu Wang, Jingzhou Chen,
Jianwei Wang, Tujun Huan, Rutai Hui. Worse prognosis with gene mutations of beta-myosin heavy chain than myosin-binding protein C in Chinese patients with hypertrophic cardiomyopathy.
Clin Cardiol. 2008;31(3):114-8.
17. Yibo Wang, Weili Zhang, Yuhui Zhang, Yuejin Yang, Lizhong Sun, Shengshou Hu, Jilin Chen,Channa Zhang, Yi Zheng, Yisong Zhen, Kai Sun, Chunyan Fu, Tao Yang,
Jianwei Wang, Jing Sun, Haiying Wu, Wayne C Glasgow, and Rutai Hui. VKORC1 Haplotypes are Associated with Arterial Vascular Diseases (Stroke, Coronary Heart Disease and Aortic Dissection).
Circulation. 2006; 113(12):1615-21.

